Das Gonadotropin-freisetzende Hormon (GnRH) ist ein Hormon, das von den Neuronen des Bogenkerns des Hypothalamus produziert wird und dann in den Portalkreislauf der Hypophyse abgegeben wird.
Seine Aufgabe ist es, die Produktion von Gonadotropinen (FSH und LH) durch die Hypophyse zu regulieren, die für das reibungslose Funktionieren des männlichen und weiblichen Fortpflanzungssystems unerlässlich ist. In den letzten Jahren wurden zahlreiche GnRH-Analoga für den Einsatz als Medikament in der assistierten Reproduktion künstlich hergestellt.
Im Anschluss finden Sie ein Inhaltsverzeichnis mit allen Punkten, die wir in diesem Artikel behandeln.
- 1.
- 2.
- 3.
- 3.1.
- 3.2.
- 3.3.
- 4.
- 4.1.
- 4.2.
- 4.3.
- 4.4.
- 4.5.
- 5.
- 6.
- 7.
Merkmale von GnRH
GnRH ist ein Dekapeptid, d.h. seine Struktur besteht aus 10 Aminosäuren, die in einer linearen Sequenz angeordnet sind. Darüber hinaus gilt GnRH, da es von Neuronen produziert wird, als Neurohormon.
Weitere relevante Merkmale sind die folgenden:
- Das Gen, das für den Vorläufer von GnRH kodiert, befindet sich auf dem kurzen Arm des Chromosoms 8.
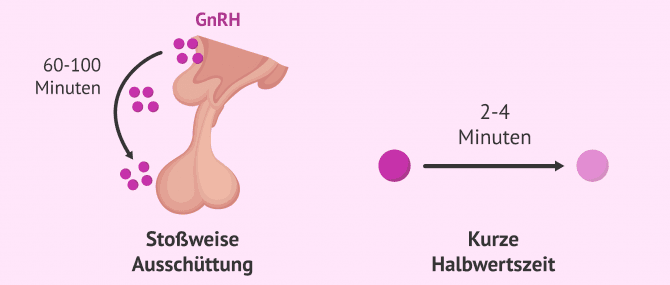
- Die Sekretion von GnRH ist pulsatil, d.h. sie wird durch Impulse unterschiedlicher Amplitude und Frequenz in das Portalsystem abgegeben.
- Seine Halbwertszeit ist sehr kurz, etwa 2-4 Minuten.
- GnRH kann im peripheren Blut nicht nachgewiesen werden, so dass es in einem normalen Bluttest nicht gemessen werden kann.
Wirkungsmechanismus
Die maximale Aktivität von GnRH beginnt mit der Pubertät und wird während des gesamten reproduktiven Lebens von Männern und Frauen aufrechterhalten.
GnRH hat eine endokrine Funktion: Es wandert über das Portalsystem zur Hypophyse, aktiviert seinen eigenen Rezeptor und stimuliert die Freisetzung von FSH und LH durch die Adenohypophyse.
Diese Hypophysenhormone wandern dann durch die Blutbahn und üben ihre Funktion auf die Eierstöcke einer Frau oder auf die Hoden eines Mannes aus.
Bei Frauen steuert die Häufigkeit der GnRH-Impulse die Produktion von FSH und LH während des gesamten Menstruationszyklus, was für einen guten Zyklus unerlässlich ist. Bei Männern hingegen wird in konstanter Häufigkeit GnRH in Impulsen ausgeschieden.
Die pulsierende Aktivität von GnRH kann durch verschiedene Faktoren unterbrochen oder verändert werden, die je nach Fall die männliche und/oder weibliche Fortpflanzungsfunktion beeinträchtigen würden. Diese sind folgende:
- Die Fehlfunktion des Hypothalamus, sei es aufgrund von Dysfunktion, Trauma oder einer Art von Tumor.
- Hyperprolaktinämie: Ein hoher Prolaktinspiegel vermindert die Aktivität von GnRH, die vor allem während der Schwangerschaft und des Stillens auftritt.
- Patientinnen mit polyzystischem Ovarialsyndrom (PCOS) und hohem Insulinspiegel, bei denen die GnRH-Pulsatilität erhöht sind, was zu einer ungeordneten LH- und FSH-Aktivität führt.
- Vom Kallmann-Syndrom betroffene Personen, die aufgrund eines Geburtsfehlers kein GnRH haben.
Auf der anderen Seite wird die Synthese von FSH und LH auch auf normale Weise gehemmt, da Androgene und Östrogene eine negative Rückkopplung auf die Hypophyse ausüben.
GnRH-Analoga
GnRH-Analoga sind eine Art von Molekül, das künstlich erzeugt wurde, indem einige Aminosäuren innerhalb des ursprünglichen GnRH-Moleküls ersetzt wurden.
Diese neuen Moleküle ahmen die Form von GnRH nach und haben auch eine starke Ähnlichkeit zu seinen Rezeptoren in der Hypophyse.
So haben GnRH-Agonisten die Fähigkeit, sich leicht an Rezeptoren zu binden und die Wirkung von natürlichem GnRH zu verhindern.
Ein Analogon ist eine Substanz mit ähnlichen Eigenschaften wie eine andere, die, ohne mit ihr identisch zu sein, einige ihrer Funktionen erfüllen kann.
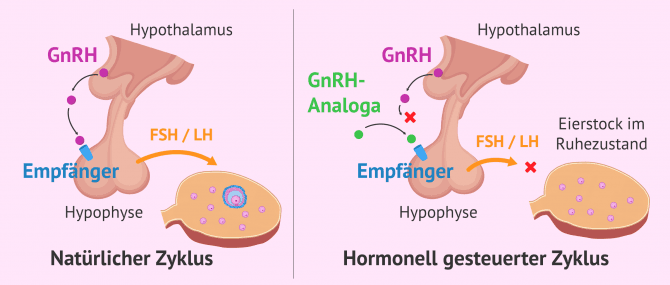
Kurz gesagt, die Wirkung von GnRH-Analoga ist es, die normale Funktion von GnRH zu blockieren und den hormonellen Fluss von FSH und LH von der Hypophyse zu den Gonaden zu verhindern.
Diese Fähigkeit der GnRH-Analoga wurde genutzt, um die Medikamente herzustellen, die während der Behandlungen der assistierten Reproduktion verabreicht werden, wie z.B. künstliche Befruchtung (IUI) oder In-vitro-Fertilisation (IVF).
Dies sind Medikamente, die während der Stimulationsphase der Eierstöcke verwendet werden, um die Hypophyse zu verlangsamen und die Eierstöcke ruhig zu halten. Auf diese Weise ist es möglich, die Anzahl der entwickelten Follikel und den Zeitpunkt des Eisprungs zu kontrollieren.
Arten
Es gibt zwei Arten von GnRH-Analoga, die sich unterschiedlich verhalten:
- GnRH-Agonisten
- haben eine längere Halbwertszeit und eine starke Ähnlichkeit zum GnRH-Rezeptor in der Hypophyse. Nach der Bindung von Agonisten und Rezeptoren kommt es zu einer plötzlichen Freisetzung von Gonadotropinen, die als Flare-Up-Effekt bezeichnet wird. Wenn GnRH-Agonisten jedoch weiterhin kontinuierlich verabreicht werden, werden die Rezeptoren schließlich blockiert und reagieren nicht mehr, so dass die Sekretion von FSH und LH ausgesetzt wird.
- GnRh-Antagonisten
- seine hemmende Wirkung ist direkter. Sobald der Antagonist am Empfänger befestigt ist, wird er sofort blockiert.
Heutzutage neigen Reproduktionsmediziner eher dazu, Follikeltimulationsprotokolle mit Antagonisten zu etablieren als mit Agonisten, da sie viele Vorteile bieten.
Effekte
Wie wir bereits erklärt haben, ist die Hauptwirkung von GnRH-Analoga auf den Körper einer Frau, die Freisetzung von Gonadotropinen durch die Adeno-Hypophyse zu blockieren.
Diese Wirkung ermöglicht die Synchronisation der Kohorte der vom Eierstock rekrutierten Follikel zu Beginn der Follikelstimulation Auf diese Weise kann ein homogenes Follikelwachstum stattfinden, das die Variabilität der Reaktion der Eierstöcke auf exogen verabreichte Gonadotropine reduziert.
Zusammenfassend lässt sich sagen, dass die Verwendung von GnRH-Analoga es dem Gynäkologen ermöglicht, den Stimulationsprozess der Follikel bei Patientinnen besser zu kontrollieren und zu wissen, wann der beste Zeitpunkt ist, um den Eisprung auszulösen und eine künstliche Insemination oder eine Follikelpunktion zu planen.
Medikamente mit GnRH-Analoga
Je nachdem, ob GnRH-Agonisten oder Antagonisten in der Phase der kontrollierten Follikelstimulation eingesetzt werden, gibt es lange bzw. kurze Protokolle.
Der Grund dafür ist, dass die Agonisten, wie wir bereits erwähnt haben, länger brauchen, um wirksam zu werden, während die Antagonisten eine sofortige Wirkung haben und weniger Einnahmetage benötigen.
Die Handelsnamen der in den langen Zyklen verwendeten Agonisten und ihrer Wirkstoffe lauten wie folgt:
- Synarel
- ist ein Nasenspray, das Nafarelin enthält.
- Procrin
- der Wirkstoff ist Leprorelinacetat und wird subkutan verabreicht.
- Decapeptyl
- je nach Art der Aufmachung, wird das Medikament subkutan oder intramuskulär verabreicht. Enthält Triptorelin als Wirkstoff.
Was die in den kurzen Zyklen verwendeten Antagonisten betrifft, so finden wir die folgenden Medikamente:
- Cetrotide
- enthält Cetrorelix und die Injektion erfolgt subkutan.
- Orgalutran
- der Wirkstoff ist Leprorelinacetat und wird subkutan verabreicht.
Wenn Sie sich über die in der assistierten Reproduktion verwendeten Medikamente informieren möchten, können Sie hier weiterlesen: Eingesetzte Medikamente bei der kontrollierten Follikelstimulation.
Fragen die Nutzer stellten
Warum kann GnRH nicht im Blut gemessen werden?
Das Gonadotropin-Releasing-Hormon (GNRH) ist ein Hormon, das von Neuronen des Hypothalamus in pulsierender Form freigesetzt wird. Es stimuliert die Freisetzung von Gonadotropinen (LH und FSH) durch die Adeno-Hypophyse.
Dieses Hormon wird schnell metabolisiert und kann daher im Blut nicht gemessen werden.
Welche GnRH-Analoga liefern die besten Ergebnisse?
Es gibt mehrere Arten von Analoga, die sich durch kleine Variationen der Komponenten des Moleküls unterscheiden. Diese wären Leprorelinacetat, Triptorelin, Nafarelin, Buserelin und Goserelin. Es gibt mehrere Präsentationen (täglich, monatlich, vierteljährlich...), die jederzeit die am besten geeignete für den gewünschten Effekt angeben. Jede Art von Analogon hat auch ihren eigenen Verabreichungsweg, der subkutan, intramuskulär oder intranasal sein kann.
Es konnte nicht nachgewiesen werden, dass einer der kommerzialisierten Agonisten einem anderen überlegen ist, obwohl der subkutane Weg eine konstante Bioverfügbarkeit und geringe Schwankungen zwischen den Patienten bietet, während die Absorption durch intranasale oder Inhalation unterschiedlicher sein kann.
Mehr lesen
Welche Wirkung haben Gonadotropin freisetzende Hormonagonisten?
Die Haupteffekte, die durch die Verwendung von GnRH-Agonistenanaloga hervorgerufen werden, sind zum einen die anfängliche Freisetzung von Gonadotropinen (Flare-up Effekt) und zum anderen die Blockade der Freisetzung dieser Gonadotropine, wodurch die Kommunikation zwischen der Hypophyse und dem Eierstock vermieden wird, so dass es zu keiner follikulären Entwicklung oder Ovulation kommt.
All dies geschieht vorübergehend, wenn die FSH- und LH-Reserve in der Hypophyse leer ist. Normalerweise tritt die totale Blockade der GnRH-Rezeptoren 5-10 Tage nach der ersten Verabreichung des Agonisten auf.
Was ist der Flare-up Effekt bei GnRH-Analoga?
Wenn das Analogon von GnRH mit seinem Rezeptor vereint ist, kommt es zu einer massiven Freisetzung der Hormone FSH (follikelstimulierendes Hormon) und LH (luteinisierendes Hormon). Dies wird als flare up Effekt bezeichnet.
Diese Freisetzung von Gonadotropinen erfolgt endogen, d.h. die im Gehirn befindliche Hypophyse synthetisiert und gibt diese Hormone an die Blutbahn ab.
Der Flare up Effekt tritt etwa zwei Tage nach der Verabreichung eines GnRH-Agonisten auf. Nach dieser Zeit wird die Hypophyse auf die anfängliche Wirkung des Agonisten desensibilisiert und die Synthese von Gonadotropinen blockiert.
Wie läuft eine Behandlung mit GnRH-Analoga bei Uterusmyomatose ab?
Obwohl die häufigste Behandlung zur Beseitigung von Myomen chirurgisch ist, können GnRH-Agonistenanaloga auch als medikamentöse Behandlung dienen, um die Größe dieser Myome zu reduzieren.
GnRH-Agonisten verursachen aufgrund ihrer Wirkung bei Frauen mit sehr niedrigen Östradiolwerten einen hypogonadotropen Hypogonadismuszustand. Dies kann dazu beitragen, Myome und mögliche Begleiterscheinungen wie Blutungen zu reduzieren.
Diese Medikamente haben jedoch unerwünschte Nebenwirkungen, und nach dem Absetzen der Behandlung können Myome wieder nachwachsen. Aus diesem Grund werden GnRH-Agonisten nur dort eingesetzt, wo es angezeigt ist und als Schritt vor der Operation, um den Eingriff zu erleichtern.
Gemeinschaft und Unterstützung
Bei inviTRA arbeiten wir daran, monatliche und fundierte Informationen für alle zugänglich zu machen. Wenn Ihnen dieser Artikel geholfen hat, unterstützen Sie uns, damit wir noch mehr Menschen auf ihrem Weg zur Elternschaft begleiten können.
Literaturverzeichnis
Depalo R, Jayakrishan K, Garruti G, Totaro I, Panzarino M, Giorgino F, Selvaggi LE. GnRH agonist versus GnRH antagonist in in vitro fertilization and embryo transfer (IVF/ET). Reprod Biol Endocrinol. 2012 Apr 13;10:26.
Gómez BP, Velázquez-Paniagua M. Fisiología de la reproducción: hormona liberadora de gonadotrofinas. Rev Fac Med UNAM, 2002; 45(6):252-257
Murillo EO, Cano A. Análogos de la GnRH en el tratamiento de los miomas. Med Clin (Barc). 2013 Jul;141 Suppl 1:35-9.
Padula AM. GnRH analogues--agonists and antagonists. Anim Reprod Sci. 2005 Aug;88(1-2):115-26.
Fragen die Nutzer stellten: 'Warum kann GnRH nicht im Blut gemessen werden?', 'Welche GnRH-Analoga liefern die besten Ergebnisse?', 'Welche Wirkung haben Gonadotropin freisetzende Hormonagonisten?', 'Was ist der Flare-up Effekt bei GnRH-Analoga?' Und 'Wie läuft eine Behandlung mit GnRH-Analoga bei Uterusmyomatose ab?'.